Quando a carga do cátion é maior do que quatro, os tetraedros de coordenação não se arranjam do modo mais compacto possível. Por exemplo, em todas as formas cristalinas da sílica, 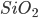 , cada átomo de silício(Si) está coordenado tetraedricamente por quatro átomos de oxigênio(O), e os tetraedros formados deste modo têm sempre dois vértices em comum. As formas alotrópicas da sílica são devidas ao fato de serem possíveis vários arranjos tridimensionais de tetraedros unidos pelos vértices.
, cada átomo de silício(Si) está coordenado tetraedricamente por quatro átomos de oxigênio(O), e os tetraedros formados deste modo têm sempre dois vértices em comum. As formas alotrópicas da sílica são devidas ao fato de serem possíveis vários arranjos tridimensionais de tetraedros unidos pelos vértices.
Na Figura 3.p.1, mostram-se células unitárias de dois desses arranjos: as estruturas cristalinas do 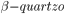 (beta quartzo) e da cristobalita. No
(beta quartzo) e da cristobalita. No 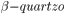 , os tetraedros estão unidos vértice a vértice, em espiral, em torno de um prisma hexagonal. Uma propriedade que é afetada pela estrutura cristalina do quartzo-beta é a transmissão de luz. Existem cristais de quartzo-beta que polarizam a luz para a direita (dextro-rotatório) e outros polarizam para a esquerda (levo-rotatório) (Figura 3.p.3).
, os tetraedros estão unidos vértice a vértice, em espiral, em torno de um prisma hexagonal. Uma propriedade que é afetada pela estrutura cristalina do quartzo-beta é a transmissão de luz. Existem cristais de quartzo-beta que polarizam a luz para a direita (dextro-rotatório) e outros polarizam para a esquerda (levo-rotatório) (Figura 3.p.3).
Na cristobalita (Figura 3.p.2), os átomos de silício estão arranjados numa rede cúbica do diamante, com os átomos de oxigênio entre cada par de átomos de silício mais próximos.
Um exemplo de coordenação octaédrica em que a carga do cátion é de quatro é o dióxido de titânio (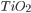 ). Os octaedros Ti—O são suficientemente grandes para que se agreguem mantendo unidas as arestas, sem que os cátions se aproximem demais uns dos outros. Entretanto, os octaedros não compartilham suas faces. Uma forma cristalográfica do (
). Os octaedros Ti—O são suficientemente grandes para que se agreguem mantendo unidas as arestas, sem que os cátions se aproximem demais uns dos outros. Entretanto, os octaedros não compartilham suas faces. Uma forma cristalográfica do (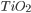 ), chamada rutilo, é mostrada na Figura 3.q.Observe que os octaedros não compartilham todas as arestas, mas apenas algumas delas.
), chamada rutilo, é mostrada na Figura 3.q.Observe que os octaedros não compartilham todas as arestas, mas apenas algumas delas.
Figura 3.p. Duas das estruturas cristalinas de 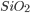 mostrando os arranjos dos tetraedros de Si—O. (3.p.1) é a estrutura cristalina do
mostrando os arranjos dos tetraedros de Si—O. (3.p.1) é a estrutura cristalina do 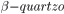 (quartzo beta), na qual duas cadeias espiraladas enrolam-se em volta de um prisma hexagonal. Os átomos de silício de uma das cadeias têm sombreado mais escuros, a fim de distingui-la da outra. (3.p.2) é a estrutura cristalina da cristobalita, na qual os tetraedros se arranjam de modo semelhante aos átomos de carbono no diamante. Os átomos de silício que estão nos pontos da rede CFC na célula unitária têm cores diferentes dos átomos de Si que se acham no interior da célula.
(quartzo beta), na qual duas cadeias espiraladas enrolam-se em volta de um prisma hexagonal. Os átomos de silício de uma das cadeias têm sombreado mais escuros, a fim de distingui-la da outra. (3.p.2) é a estrutura cristalina da cristobalita, na qual os tetraedros se arranjam de modo semelhante aos átomos de carbono no diamante. Os átomos de silício que estão nos pontos da rede CFC na célula unitária têm cores diferentes dos átomos de Si que se acham no interior da célula.
Figura 3.p. Beta-Quartzo e Cristobalita: Fases da Sílica
Figura 3.q O arranjo dos octaedros Ti-O de coordenação na estrutura rutilo de 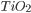 Note-se que a célula é tetragonal e que os octaedros compartilham vértices e arestas, mas não faces.
Note-se que a célula é tetragonal e que os octaedros compartilham vértices e arestas, mas não faces.