A superfície de um corpo ou de uma fase são regiões de fronteira (Figura 12.a) e possuem propriedades que as distinguem do interior do corpo ou do interior das fases. As interfaces estão repletas de ligações interrompidas e, devido a este fato, existe um excesso de energia de superfície 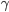 , que é medida em energia por unidade de área da superfície.
, que é medida em energia por unidade de área da superfície.
Na interface entre duas fases ou dois corpos, o estado de agregação dos átomos e a composição química variam de um modo abrupto. Os átomos da superfície não se encontram em equilíbrio, pois não estão nem em um corpo nem em outro, nem em uma fase nem em outra. Existe uma abundância de ligações não satisfeitas, de nuvens eletrônicas distorcidas porque os átomos da superfície perderam alguns dos primeiros vizinhos. A energia em excesso tem relação com o número de átomos que compõe a superfície e é, portanto, proporcional à área superficial.
Por convenção, utiliza-se o termo superfície para a fronteira que separa duas fases, sendo uma delas gasosa. Também por convenção, a fronteira entre duas fases não-gasosas é chamada de interface. Quando se trata de fases num sólido, existem os contornos de grão, que são superfícies entre grãos de orientações cristalográficas distintas.
As superfícies são importantes no estudo das microestruturas, no estudo do atrito e do desgaste (1), da junção de quaisquer materiais por quaisquer processos, da catálise das reações químicas, da oxidação, da corrosão, do comportamento mecânico de corpos muito pequenos ou muito finos, de dispositivos eletrônicos, enfim, no estudo de uma grande variedade de outros fenômenos.
Figura 12.a – Variação da coordenação dos átomos nas superfícies.O número de primeiros vizinhos(2) de um átomo do interior de um sólido é maior do que o número de primeiros vizinhos de um átomo da sua superfície. O número de coordenação também é diferente entre o interior do sólido e a interface sólido-líquido; ou entre o interior do sólido e do líquido e as superfícies do tipo sólido-gás e do tipo líquido-gás.