Um dos tipos de diagramas de equilíbrio que podem existir quando há apenas uma solubilidade limitada (Veja Tópico 8.10) no estado sólido é o diagrama eutético binário, apresentado esquematicamente na Figura 8.l. Considere a liga 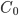 , que apresenta uma única fase líquida no ponto a; quando é resfriada até o ponto b, a composição do primeiro sólido a se formar é dada pela outra fronteira da região de duas fases, ponto
, que apresenta uma única fase líquida no ponto a; quando é resfriada até o ponto b, a composição do primeiro sólido a se formar é dada pela outra fronteira da região de duas fases, ponto 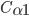 . Resfriando-se até o ponto c, tem-se, em equilíbrio, uma fase sólida de composição
. Resfriando-se até o ponto c, tem-se, em equilíbrio, uma fase sólida de composição 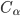 e um líquido de composição
e um líquido de composição 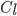 . Como no caso do diagrama de solução sólida, as quantidades relativas das duas fases em equilíbrio podem ser calculadas pela regra da alavanca. No ponto c, a fração da liga que é
. Como no caso do diagrama de solução sólida, as quantidades relativas das duas fases em equilíbrio podem ser calculadas pela regra da alavanca. No ponto c, a fração da liga que é  é dada por
é dada por 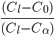 e a fração que é líquido é dada por
e a fração que é líquido é dada por 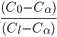 . As regiões superiores com duas fases,
. As regiões superiores com duas fases, 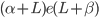 , da Figura 8.j, podem ser consideradas partes de um par de diagramas de soluções sólidas, um para a solução de B em A e outro para a solução de A em B.
, da Figura 8.j, podem ser consideradas partes de um par de diagramas de soluções sólidas, um para a solução de B em A e outro para a solução de A em B.
Continuando o resfriamento do material abaixo do ponto c, mais sólido se forma e a composição do líquido varia segundo a linha liquidus até o ponto e, que é chamado ponto eutético. Com uma retirada adicional de calor do sistema, o líquido eutético de composição 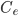 se solidifica isotermicamente, na temperatura eutética
se solidifica isotermicamente, na temperatura eutética 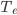 . Esta transformação de fase é denominada reação eutética. É um ponto invariante do sistema; como as três fases estão em equilíbrio durante a solidificação do líquido eutético, não há nenhum grau de liberdade. A temperatura, a composição da fase líquida e as composições de ambas as fases sólidas são fixas.
. Esta transformação de fase é denominada reação eutética. É um ponto invariante do sistema; como as três fases estão em equilíbrio durante a solidificação do líquido eutético, não há nenhum grau de liberdade. A temperatura, a composição da fase líquida e as composições de ambas as fases sólidas são fixas.
Figura 8.l – Diagrama de equilíbrio binário hipotético para os elementos A e B que são completamente solúveis em todas as proporções no estado líquido, mas apenas parcialmente solúveis no estado sólido. 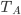 e
e  são os pontos de fusão de A puro e B puro;
são os pontos de fusão de A puro e B puro; 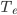 é a temperatura eutética.
é a temperatura eutética.