Camada eletrônica: um grupo de elétrons que têm o mesmo número quântico principal n; muitas vezes designada por letras maiúsculas, como camada K para n = 1, camada L para n = 2, etc.
Caroço iônico: um átomo sem seu (seus) elétron (elétrons) de valência.
Distância de equilíbrio: a distância interatômica, na qual a força de atração iguala a força de repulsão entre dois átomos.
Elétrons de valência: elétrons da camada mais externa que tomam parte na ligação.
Estado fundamental: o estado quântico de mais baixa energia.
Força de ligação: a força que mantém juntos dois átomos; resulta de um decréscimo de energia quando dois átomos se aproximam um do outro.
Função de onda:  , a solução da equação de onda de Schrödinger.
, a solução da equação de onda de Schrödinger.
Função de probabilidade do elétron: 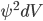 , a probabilidade de achar-se um elétron num elemento de volume dV.
, a probabilidade de achar-se um elétron num elemento de volume dV.
Hibridização: rearranjo com a combinação de orbitais. O fenômeno é acompanhado por uma grande extensão espacial dos orbitais, que facilita a interseção destes no momento da ligação e produz orbitais direcionais.
Ligação covalente: ligação primária e direcional que reduz a energia dos átomos envolvidos ao permitir a superposição de orbitais semipreenchidos de dois átomos. Os elétrons destes orbitais são então compartilhados pelos átomos envolvidos na ligação.
Ligação de dipolo permanente: ligação que decorre da atração entre dipolos, cujas extremidades opostas carregadas são átomos eletronegativos e eletropositivos.
Ligação de van der Waals: ligação que resulta da ocorrência de dipolos numa molécula ou num átomo. Dipolos-dipolos podem ocorrer entre moléculas cuja ligação iônica resulta em uma molécula com pólo positivo e negativo, (forças de Keesom); podem ser induzidos por uma molécula polar sobre outra apolar, (forças de Debye); e dipolo flutuante de um átomo não-polar, que tem totalmente preenchidas as camadas eletrônicas ocupadas (forças de dispersão).
Ligação de hidrogênio: ligação que resulta das atrações entre dipolos, quando o hidrogênio é a extremidade positiva do dipolo. É uma ligação direcional.
Ligação iônica: ligação primária decorrente da atração eletrostática entre dois íons de cargas de sinais opostos.
Ligação metálica: ligação primária decorrente da difusão, para o espaço interatômico, dos elétrons de valência, quando um certo número de átomos metálicos é agrupado.
Mecânica Ondulatória: ramo da Física Teórica que desenvolveu e desenvolve expressões matemáticas (em geral, equações diferenciais) que descrevem o comportamento das ondas.
Mecânica Quântica: ramo da Física Teórica que desenvolveu um conjunto de teorias matemáticas para descrever as propriedades de partículas subatômicas, átomos e moléculas.
Números quânticos: conjunto de números inteiros (n, l, m), representando as soluções discretas da equação de onda de Schrödinger, independente do tempo; valores permitidos de cada um são dados na Tab. 1.1, Tópico 1.2. O número quântico de spin, 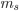 , pode ser incluído para indicar o spin do elétron (
, pode ser incluído para indicar o spin do elétron (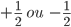 ).
).
Orbital: descrição matemática da Mecânica Quântica para o estado do elétron, incluindo sua energia e sua distribuição espacial média no tempo.
Princípio da incerteza: proposição que estabelece que medições simultâneas de pares conjugados de variáveis, como quantidade de movimento e posição, ou energia e tempo, estão sujeitas a uma indeterminação específica; também chamado princípio de indeterminação.
Princípio de exclusão de Pauli: postulado da Mecânica Quântica que prediz que, no máximo, dois elétrons podem ocupar o mesmo orbital e que, se houver dois elétrons, eles devem ter spins opostos.
Saltos quânticos: conceito da Mecânica Quântica para descrever a variação da energia de um estado permitido para outro.