Uma imperfeição pontual é uma interrupção muito localizada na regularidade da rede. Como regra, uma imperfeição pontual aparece por causa da ausência de um átomo da matriz (que estaria presente num cristal perfeito) ou a presença de um átomo de impureza, ou um átomo da matriz colocado em lugar “errado” (um sítio não ocupado no cristal perfeito). Na Figura 5.a mostram-se as imperfeições pontuais mais comuns num cristal de um elemento puro; algumas das imperfeições pontuais que podem ocorrer num cristal iônico são mostradas na Figura 5.b. A ausência de um átomo numa posição normalmente ocupada é chamada de lacuna ou vacância. Um átomo estranho, que ocupa o lugar de um átomo da matriz, é chamado átomo de impureza substitucional, e um átomo estranho situado num interstício entre átomos da matriz é chamado átomo de impureza intersticial. Além disso, há imperfeições pontuais mais complexas, por exemplo, grupos de lacunas condensadas como bi-lacunas (duas lacunas juntas) e tri-lacunas (três lacunas juntas).
Em cristais iônicos, um pequeno cátion pode abandonar seu sítio, criando uma lacuna catiônica, e ficando dissolvido intersticialmente na estrutura; este par de defeitos associados (uma lacuna catiônica e um cátion intersticial) é chamado imperfeição de Frenkel. Quando uma lacuna catiônica é associada à lacuna aniônica, ao invés de um cátion intersticial, o par (lacunas aniônica e catiônica associadas) é chamado imperfeição de Schottky. Em geral, é mais provável que se formem imperfeições Schottky do que imperfeições Frenkel, porque são poucas as estruturas que contêm interstícios suficientemente grandes para dissolver cátions sem deformação considerável. Entretanto, numa estrutura relativamente aberta como a da fluorita (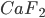 ) (1), onde os interstícios são grandes, é muito provável que os cátions se dissolvam intersticialmente e produzam imperfeições Frenkel.
) (1), onde os interstícios são grandes, é muito provável que os cátions se dissolvam intersticialmente e produzam imperfeições Frenkel.
Além das imperfeições estruturais, outras imperfeições pontuais, que não são de natureza estrutural e podem ser produzidas pela excitação de elétrons, em certos átomos, até níveis de energia superiores. Isto pode ser obtido pelo bombardeamento do cristal com feixe de elétrons (produzindo-se raios X), com radiação de microondas (o princípio dos “masers” (2)), lasers (3) e outras formas de radiação com freqüência adequada.
Figura 5.b – Uma representação bidimensional de um sólido iônico, ilustrando várias das possíveis imperfeições pontuais. Os cátions são representados por pequenas esferas, e os ânions por grandes esferas.